Tabla de Contenidos
Kovalent yarıçap kavramı, başka bir atomla kovalent bir bağın parçası olduğunda bir atomun boyutuyla ilgilidir. Şekilde görüldüğü gibi, kovalent yarıçap, bir kovalent bağı paylaşan iki atomun çekirdekleri arasındaki mesafenin yarısı olarak tanımlanır. Kovalent yarıçap, pikometre (pm) veya angstrom (Å) (1 Å = 100 pm) birimleriyle ifade edilir. Bir atomun kovalent yarıçapı, diğer atomlarla ilişkisi açısından tanımlandığından, değeri benzersiz değildir ve diğer atomlarla olan bağına bağlı olacaktır; Daha sonra göreceğimiz gibi, bir elementin kovalent yarıçapı, tekli kovalent bağla veya ikili veya üçlü kovalent bağla birleştiğinde farklıdır.
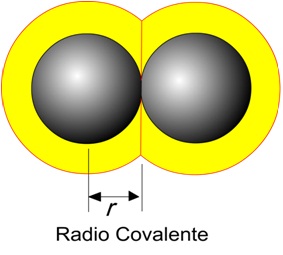
Atom yarıçapı, iyonik yarıçap, metalik yarıçap ve kovalent yarıçap
Bir elementin atomik yarıçapı kavramı, çekirdeği ile en uzaktaki elektronlar arasındaki mesafe ile ilişkilidir. Atomun şekli diğer atomlarla bağlanırken değişebilir, bu nedenle atom yarıçapı tutarlı bir şekilde tanımlanmış bir fiziksel parametre değildir ve bu nedenle atomun kimyasal bağına bağlı olarak farklı yarıçaplar tanımlanır. Genel olarak, bir kimyasal elementin atom yarıçapı, çekirdeği ile kimyasal olarak bağlı olduğu başka bir atom arasındaki mesafenin yarısı olarak tanımlanabilir.. Daha önce gördüğümüz gibi, kovalent yarıçap, atom bir kovalent bağ ile bağlandığında atomik yarıçapla aynı şekilde tanımlanır ve iyonik yarıçap, kristal bir kafeste olduğu gibi, atom bir iyonik bağ kurduğunda atomik yarıçap olacaktır. bir tuz. Aynı şekilde, metalik yarıçap tanımlanıratomlar metalik bir bağ ile bağlandığında atom yarıçapı olarak. Örneğin, sodyum (Na) durumunda, atom yarıçapı 180 pm, kovalent yarıçap 154 pm ve metalik yarıçap 186 pm’dir. Kalsiyum (Ca) durumunda, atom yarıçapı da 180 pm, tek bağ ile kovalent yarıçap 174 pm, üçlü bağ ile kovalent yarıçap 133 pm ve metalik yarıçap 197 pm’dir. Diğer bir örnek, atom yarıçapı 140 pm, tek bağ ile kovalent yarıçap 125 pm, üçlü bağ ile kovalent yarıçap 102 pm ve metalik yarıçap 126 pm olan demirin (Fe) örneğidir.
kaynaklar
- Pyykko, P., Atsumi, Elementler için M. Moleküler Tek Bağ Kovalent Yarıçaplar 1-118 . Kimya: Bir Avrupa Dergisi 15: 186–197, 2009. doi: 10.1002/chem.200800987
- Sanderson, RT Elektronegatiflik ve Bağ Enerjisi . Journal of the American Chemical Society 105 (8): 2259–2261, 1993. doi: 10.1021/ja00346a026



