Tabla de Contenidos
El CCl4 es un líquido tóxico de bajo punto de fusión y ebullición que ha sido utilizado a lo largo de los años en un gran número de aplicaciones tales como refrigeración, plaguicidas, fungicidas y extinción de incendios, entre otras.
Este compuesto ha recibido varios nombres distintos según la industria en la cual se ha utilizado. Además, se puede nombrar de diferentes maneras en los distintos sistemas de nomenclatura química, según se considere como un compuesto orgánico o inorgánico.
Es por esto que comenzaremos esta explicación analizando qué tipo de compuesto es el CCl4, qué tipo de enlaces posee y cuáles son las principales características estructurales que le proporcionan sus propiedades características.
Estructura del CCl4
Tipo de enlace en el CCl4
Para empezar, se debe tomar en cuenta el hecho de que el CCl4 está formado por 4 átomos de cloro y uno de carbono. Ambos son elementos no metálicos que forman parte del bloque p de la tabla periódica. El cloro es un halógeno con número atómico 17. Es un elemento electronegativo (tiene una electronegatividad de 3,0) bastante reactivo que tiende a reducirse a ion cloruro.
El carbono, por otro lado, es un no metal de número atómico 6 y forma la base de la química orgánica y de la vida tal como la conocemos. Es un elemento ligeramente electronegativo (2,5) que tiende a formar 4 enlaces para poder llenar su octeto.
Como la diferencia de electronegatividad entre ambos elementos es de 0,5, entonces el enlace C-Cl se clasifica como un enlace covalente polar, con su momento dipolar apuntando hacia el átomo de cloro.
Geometría molecular
En la estructura de Lewis del CCl4, el átomo de carbono va en el centro (ya que es el menos electronegativo de los dos) y está rodeado de los 4 átomos de cloro por medio de enlaces covalentes simples.
En base a la teoría de repulsión de los pares electrónicos de valencia, esta configuración asume una geometría tetraédrica regular, ya que los cuatro grupos que rodean al carbono son exactamente iguales entre sí.
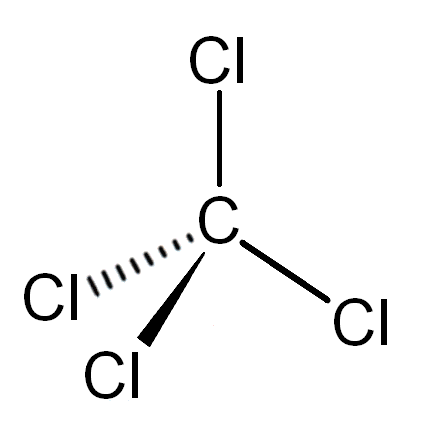
Polaridad del CCl4
Los enlaces entre el carbono y los átomos de cloro podrán ser enlaces polares y poseer un momento dipolar, pero, debido a la alta simetría de la molécula de CCl4, todos los momentos dipolares se cancelan entre sí para dar una molécula completamente apolar.
Esto, junto con el hecho de ser un líquido a temperatura ambiente, hace del CCl4 un excelente solvente apolar utilizado ampliamente tanto en la industria como en los laboratorios de química orgánica.
¿Es un compuesto orgánico o inorgánico?
Una de las razones por las que el CCl4 posee varios nombres es debido al hecho de que algunos lo consideran como un compuesto inorgánico mientras que otros lo consideran orgánico.
Los que defienden que el CCl4 es un compuesto inorgánico lo clasifican como un tipo de compuesto binario denominado pseudosal. Esta denominación sugiere que el enlace entre los dos elementos es de tipo iónico, cosa que sabemos que no es así. Sin embargo, el hecho de estar formado por la unión de dos elementos no metálicos, uno siendo un halógeno y el otro no, le da algo de fuerza a este argumento.
Por otro lado, el hecho de que es un compuesto covalente con un átomo de carbono en su centro hace que muchos lo consideren como un compuesto orgánico. Sumado a esto está el hecho de que es un solvente utilizado con frecuencia en química orgánica, y que se puede incluir en la familia de los halogenuros de alquilo (también llamados haloalcanos).
Está claro que el CCl4 se acerca más a los compuestos orgánicos que a los inorgánicos, sin embargo, se suele nombrar como uno o como el otro de manera intercambiable.
El nombre del CCl4
Ahora que tenemos más información acerca de las características del CCl4 podremos entender con mayor facilidad los distintos nombres por los que se le conoce.
Nombre en química orgánica
Al considerarse como un compuesto orgánico, el CCl4 se nombra como un derivado del alcano de un solo átomo de carbono, es decir, del metano. En química orgánica este compuesto recibe dos nombres diferentes:
- Tetraclorometano (nomenclatura IUPAC)
- Perclorometano
- Tetracloruro de metilo
El primer nombre se construye siguiendo las reglas de la nomenclatura IUPAC para los halogenuros de alquilo. Se nombra primero los sustituyentes (los 4 cloros) precedidos de su localizador (lo que en este caso no es necesario ya que solo hay 1 carbono) y finamente el nombre de la cadena principal (en este caso metano). El prefijo tetra indica que hay cuatro cloros como sustituyentes.
En el segundo nombre, en lugar de utilizar el prefijo tetra que significa, literalmente, cuatro, se utiliza el prefijo per-. Percloro- indica que todos los átomos de hidrógeno fueron reemplazados por átomos de cloro. Como el metano originalmente tenía 4 hidrógenos, percloro- significa que este compuesto tiene 4 cloros.
El tercer nombre corresponde al nombre típico de un haluro de alquilo
Nombre como compuesto binario inorgánico
Como se mencionó anteriormente, en química inorgánica se nombra este compuesto (considerado una pseudosal) como si fuera una sal iónica normal. Se nombra siempre al anión primero (en este caso el cloruro) y luego al catión (en este caso un carbono). Hay tres sistemas de nomenclatura para este tipo de compuestos en química inorgánica:
- Cloruro carbónico (nomenclatura tradicional)
- Cloruro de carbono (IV) (nomenclatura Stock)
- Tetracloruro de carbono (nombre IUPAC)
El nombre tradicional identifica la valencia del carbono a través del prefijo –ico, el cual indica que está trabajando con la mayor de sus dos valencias que es +4.
El nombre Stock simplifica las cosas, colocando directamente la valencia del carbono en números romanos y entre paréntesis.
Finalmente, el nombre sistemático IUPAC indica cuántos cloros y carbonos contiene el compuesto por medio de un sistema de prefijos. Este es el nombre más comúnmente utilizado para el CCl4.
Otros nombres comunes
Además de estos nombres, existen otros sinónimos para el tetracloruro de carbono. En la agricultura y en las lavanderías al seco se conoce a este solvente como Halo 104. El 1 indica que posee un solo carbono, el 0 en la segunda posición indica que no contiene ningún átomo de flúor y el 4 en la tercera posición indica que posee 4 átomos de cloro.
En la industria de la refrigeración se le conoce como Freón-10 (PCC-10) o Refrigerante-10 (R-10). Además, también se le conoce como carbon tet y benziform.
Referencias
Nomenclature of Alkyl Halides. (2019, June 5). Recuperado de https://chem.libretexts.org/@go/page/28165
International Union of Pure and Applied Chemistry (2005). NOMENCLATURE OF INORGANIC CHEMISTRY
IUPAC Recommendations.
Leigh O., G.J., Favre, H.A., Metanomski, W.V. (1998). Principles of chemical nomenclature: a guide to
IUPAC recommendations. Recuperado de https://old.iupac.org/publications/books/principles/principles_of_nomenclature.pdf



